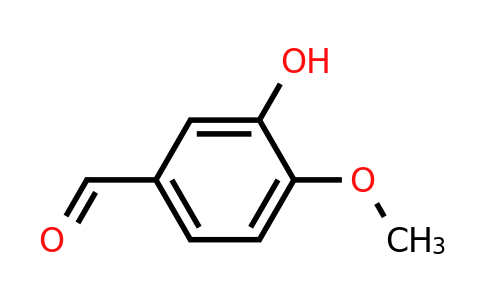
L'isovanilline est un composé aromatique de formule C8H8O3. Elle est constituée d'un cycle de benzène substitué par un groupe aldéhyde, un groupe méthoxyle (-OCH3) et un groupe hydroxyle. Comme son nom l'indique, c'est un isomère de la vanilline, dont elle ne diffère que par l'inversion de position des groupes hydroxyle et méthoxyle. Elle fait ainsi partie du groupe des isovanilloïdes, les composés isomères des vanilloïdes. C'est un composé utilisé en synthèse dans les industries cosmétique, agroalimentaire et pharmaceutique.
Occurrence naturelle
L'isovanilline a été isolée et caractérisée en 1882 par Rudolf Wegscheider, un chimiste autrichien. Elle est notamment présente dans le manioc et Mondia whitei,.
Propriétés
L'isovanilline se présente sous la forme d'une poudre marron clair, qui fond vers 113–115 °C et bout vers 179 °C à pression réduite (20 hPa). Elle est légèrement soluble dans l'eau chaude mais quasiment insoluble dans l'eau froide ; elle est soluble dans le chloroforme, l'éthanol, l'éther, le méthanol et l'acide acétique glacial. Elle cristallise dans le système monoclinique et le groupe d'espace P21/a (no = 14), de paramètres a = 851,7 pm, b = 1338,0 pm, c = 639,0 pm, β = 97,21° avec quatre unités par maille.
L'isovanilline dérive structurellement du benzaldéhyde et du gaïacol. C'est un isomère de position de la vanilline où les groupes méthoxyle et hydroxyle sont inversés. Contrairement à la vanilline, l'isovanilline est quasiment inodore.
Elle est soluble dans une solution de chlorure de fer(III) mais ne forme aucune couleur. Le pKA de son groupe phénol est de 8,89 (25 °C), plus faible que celle du phénol (9,99). Cela s'explique par l'effet -M du groupe aldéhyde qui stabilise légèrement la forme déprotonée.
L'isovanilline est un inhibiteur sélectif de l'aldéhyde oxydase. Ce n'est pas un substrat de cette enzyme et elle est métabolisée en acide isovanillique par l'aldéhyde déshydrogénase,,,,.
Extraction et synthèse
Extraction de l'isovanilline naturelle
L'isovanilline peut être extraite par divers solvants mais aussi par entraînement à la vapeur à partie des racines séchées de Mondia whitei,,.
Synthèse
Il existe de nombreuses méthodes de synthèse de l'isovanilline :
- Réaction de l'héliotropine (1,3-benzodioxole-5-carbaldéhyde) avec l'éthanolate de sodium en présence de chlorure de cuivre(I) dans le diméthylformamide ;
- Déméthylation sélective du vératraldéhyde (3,4-diméthoxybenzaldéhyde) par la méthionine dans l'acide méthylsulfonique. La réaction est lente, et la sélectivité est faible.
- L'O-méthylation sélective du protocatéchualdéhyde (3,4-dihydroxybenzaldéhyde) par l'iodométhane en présence d'hydrure de sodium dans le diméthylsulfoxyde a un rendement d'environ 65 %.
- Formylation du gaïacol (o-méthoxyphénol), protégé sous forme d'acétate, par le dichloro(méthoxy)méthane en présence de tétrachlorure de titane dans le dichlorométhane. Le 3-acétoxy-4-méthoxybenzaldéhyde est ensuite hydrolysé par l'hydroxyde de sodium.
- L'isovanilline peut être obtenue avec de bons rendements par clivage sélectif d'un 3-alcoxy-4-méthoxybenzaldéhyde par action d'un acide fort sur le groupe alkyle en position 3 ; le groupe alcoxyle doit comporter au moins deux atomes de carbone. Il est par exemple possible de partir de l'éthylvanilline (1), qui est alors méthylée par le sulfate de diméthyle (DMS) pour former le 3-éthoxy-4-méthoxybenzaldéhyde (2), qui est ensuite clivé sélectivement par l'acide sulfurique en isovanilline (3) :
Utilisations
L'isovanilline est utilisée comme « bloc de construction » pour la synthèse d'autres composés dans les industries pharmaceutique, cosmétique et agroalimentaire,,,. L'isovanilline est par exemple un précurseur dans la synthèse totale de la morphine,.
Dérivés structurels
L'alcool isovanillique (3-hydroxy-4-méthoxybenzylalcool) est produit par réduction de l'isovanilline. L'acide isovanillique (acide 3-hydroxy-4-méthoxybenzoïque) est produit par oxydation, par exemple par voie enzymatique.
L'isoéthylvanilline (3-hydroxy-4-éthoxybenzaldéhyde) est un dérivé structurel de l'isovanilline, obtenu en remplaçant le groupe méthyle par un groupe éthyle. La relation entre les deux composés est analogue à celle entre la vanilline et l'éthylvanilline.
L'isoacétovanillone (3-hydroxy-4-méthoxyacetophénone) est similaire à l'isovanilline, en remplaçant le groupe aldéhyde par un groupe acétyle. La relation entre les deux composés est analogue à celle entre la vanilline et l'acétovanillone (apocynine).
Notes et références
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « Isovanillin » (voir la liste des auteurs).
- Portail de la chimie